Tổng quan: Đái tháo đường (ĐTĐ) là một bệnh rối loạn chuyển hóa đặc trưng bởi tình trạng tăng glucose huyết mạn tính. Việc tìm kiếm các chất ức chế α-glucosidase mới với tiềm năng hiệu quả cao và ít tác dụng phụ là một lĩnh vực nghiên cứu rất được quan tâm. Trong bối cảnh đó, cây Súng đỏ (Nymphaea rubra Roxb. ex Andrews) đã được lựa chọn làm đối tượng nghiên cứu chính cho đề tài này. Các nghiên cứu đã chỉ ra rằng dịch chiết từ cây Súng đỏ có khả năng ức chế enzym α-glucosidase, điều này gợi ý tiềm năng chứa các hợp chất giá trị. Sàng lọc ảo giúp tiết kiệm thời gian và chi phí khi tìm các hợp chất phù hợp có khả năng ức chế enzym α-glucosidase.
I. Đặt vấn đề
Đái tháo đường (ĐTĐ) là gánh nặng kinh tế toàn cầu và được dự báo nằm trong top 7 nguyên nhân tử vong hàng đầu tại Việt Nam vào năm 2030 [1]. ĐTĐ là bệnh rối loạn chuyển hóa đặc trưng bởi tình trạng tăng glucose huyết mạn tính [2], một chiến lược điều trị ĐTĐ hiệu quả là kiểm soát sự hấp thu carbohydrate sau bữa ăn. Điều này có thể đạt được thông qua việc ức chế hoạt động của các enzym tiêu hóa chính như α-glucosidase, làm chậm quá trình giải phóng glucose vào máu [3]. Tuy nhiên, các thuốc ức chế α-glucosidase hiện hành như Acarbose, Voglibose và Miglitol lại gặp hạn chế về tác dụng phụ trên đường tiêu hóa [4], từ đó thúc đẩy nhu cầu tìm kiếm các chất ức chế hiệu quả và an toàn hơn.
Trong bối cảnh đó, cây Súng đỏ (Nymphaea rubra Roxb. ex Andrews) đã được lựa chọn làm đối tượng nghiên cứu chính cho đề tài này. Dịch chiết cây Súng đỏ được báo cáo có khả năng ức chế α-glucosidase, cho thấy chứa các hợp chất có tiềm năng kiểm soát đường huyết [5-6]. Do đó, nhằm góp phần tìm kiếm các chất có hoạt tính tốt phù hợp để phát triển thành thuốc và khai thác tiềm năng trị liệu của loài cây này đối với bệnh ĐTĐ, nhóm nghiên cứu tiến hành đề tài: “Nghiên cứu sàng lọc in silico các hợp chất phân lập từ cây Súng đỏ (Nymphaea rubra Roxb. ex Andrews) có khả năng ức chế enzym α-glucosidase” với ba mục tiêu:
- Mục tiêu 1: Xây dựng mô hình mô tả phân tử docking trên enzym α-glucosidase và sàng lọc các hợp chất tiềm năng được phân lập từ cây Súng đỏ (Nymphaea rubra Roxb. ex Andrews) có khả năng ức chế enzym bằng phương pháp docking.
- Mục tiêu 2: Sàng lọc các hợp chất tiềm năng có khả năng ức chế enzym α-glucosidase bằng phương pháp đánh giá ADMET.
- Mục tiêu 3: Đánh giá các hợp chất tiềm năng có khả năng ức chế enzym α-glucosidase thông qua mô hình mô phỏng động lực học phân tử.
II. Đối tượng và phương pháp nghiên cứu
2.1. Đối tượng nghiên cứu
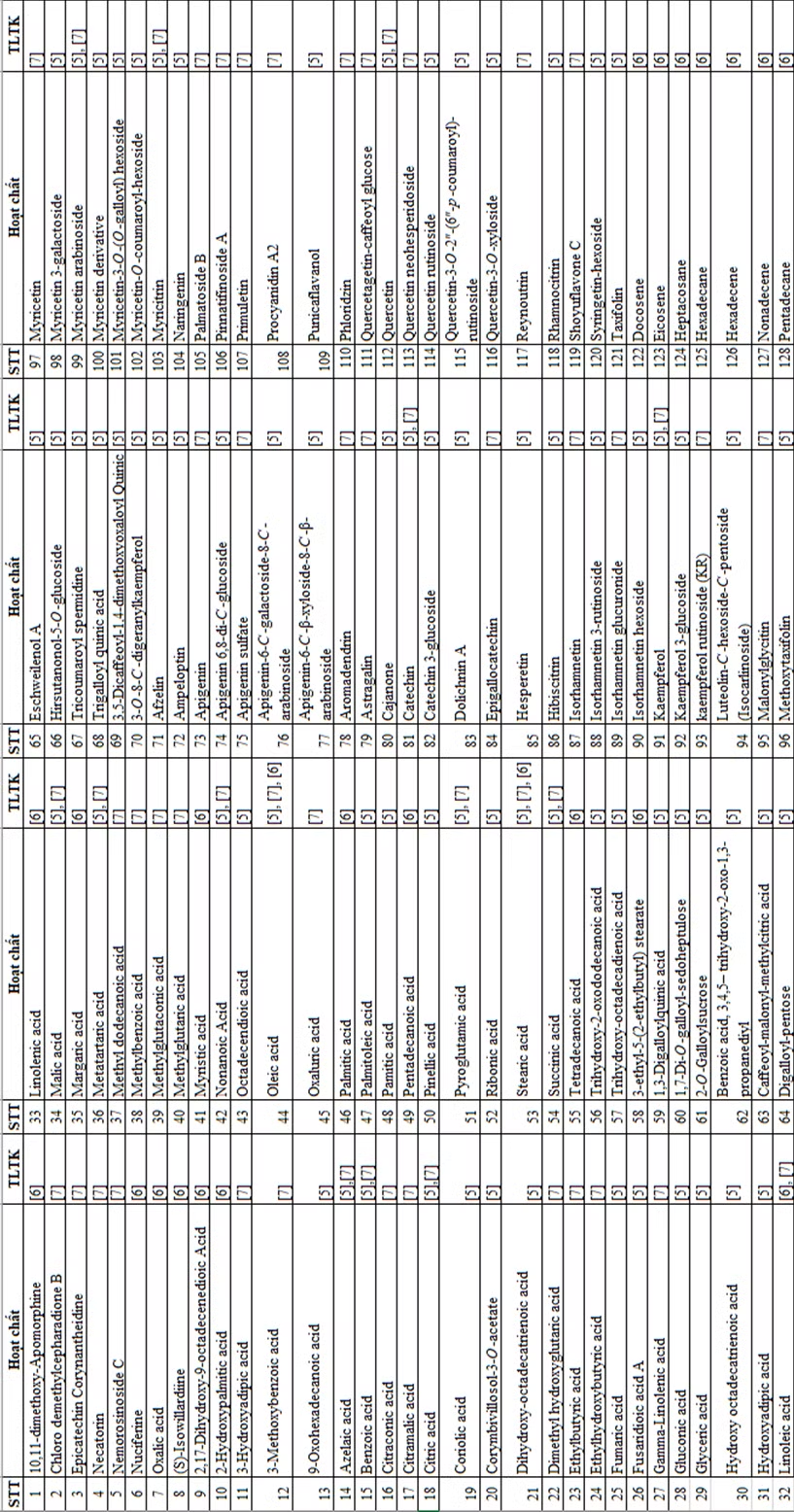
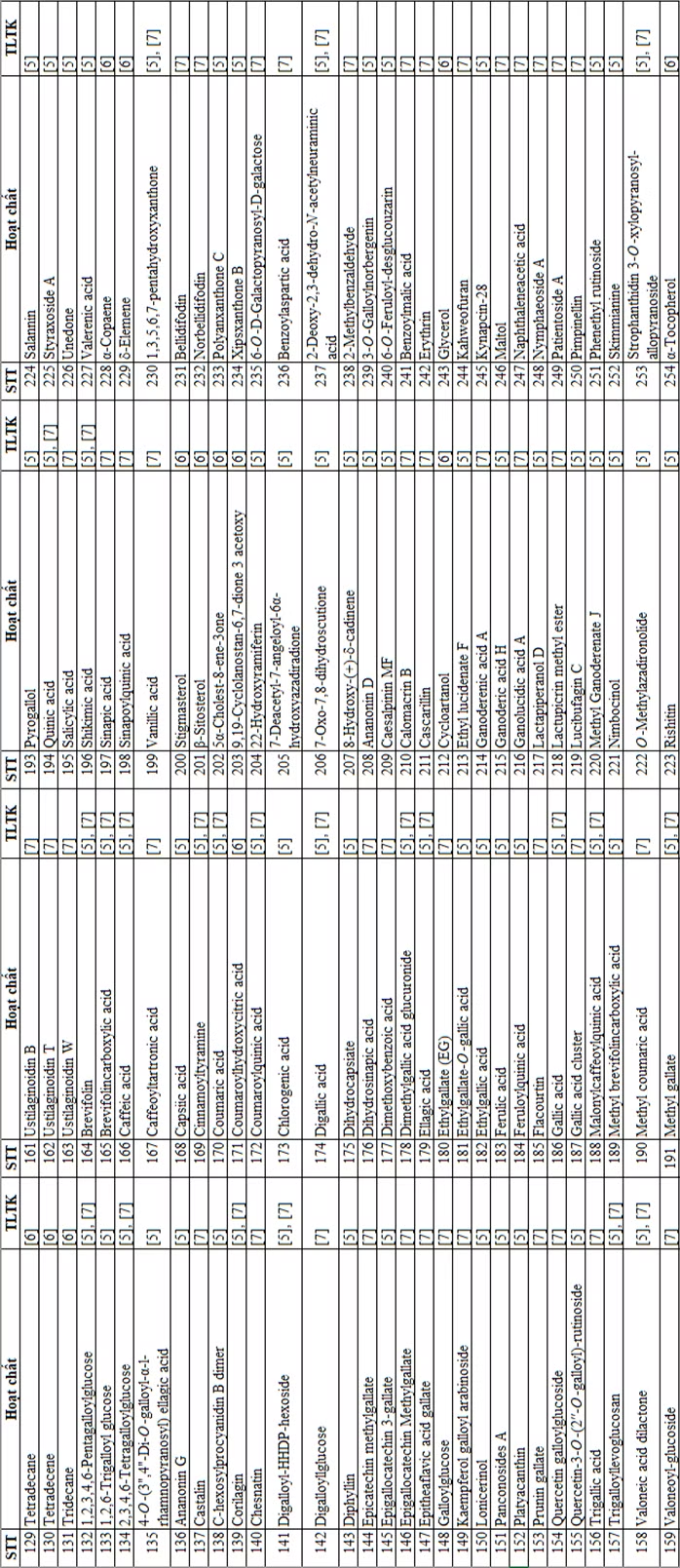
- Cấu trúc phối tử: 254 hợp chất được phân lập từ cây Súng đỏ (Phụ lục 2) [5-7].
- Cấu trúc thụ thể: Cấu trúc tia X của enzym α-glucosidase được lấy từ ngân hàng dữ liệu Protein châu Âu RCSB [8] với mã ID: 2QMJ (độ phân giải 1.90 Å) [9].
2.2. Phương pháp nghiên cứu
2.2.1. Khảo sát mô hình Docking
2.2.1.1. Chuẩn bị cấu trúc protein và phối tử
Cấu trúc các protein: Cấu trúc protein 3D được tải từ RCSB (.pdb) [8], loại bỏ phối tử đi kèm và nước bằng BIOVIA Discovery Studio 2024, sau đó thêm hydro và lưu dưới dạng .pdbqt bằng AutoDock Tools v1.5.7.
Cấu trúc phối tử: Cấu trúc phối tử 3D được xác định và tải xuống từ cơ sở dữ liệu Pubchem [10]. Những phối tử không truy cập được từ trang web cũng sẽ được vẽ lại từ phần mềm Chem3D. Cấu trúc 3D sau cùng được lưu dưới dạng .pdb.
2.2.1.2. Tiến hành re-docking và docking
Quá trình re-docking bằng AutoDock Vina được thực hiện nhằm đánh giá độ tin cậy và khả năng tái tạo dữ liệu thực nghiệm. Kết quả được xem là đáng tin cậy khi RMSD của cấu dạng ligand sau khi tái gắn kết so với cấu dạng ban đầu ≤ 2 Å [11] và các tương tác ligand-protein không khác biệt đáng kể so với cấu trúc gốc [12]. Thông số tọa độ gắn kết cho hệ 2QMJ: x = –21.727, y = –6.323, z = –5.281; kích thước hộp: 22×20×22 Å [13-15].
2.2.1.3. Phân tích kết quả
Điểm số gắn kết được biểu thị bằng năng lượng tự do liên kết (ΔG, kcal/mol) giá trị càng âm thể hiện ái lực gắn kết càng cao. So sánh với ngưỡng điểm và vị trí liên kết của Acarbose với protein đích, chọn ra các hợp chất tiềm năng.
2.2.2. Đánh giá ADMET
Cấu hình ADMET được dự đoán bằng công cụ ADMETlab 3.0 [16] và pkCSM [17].
2.2.3. Mô phỏng động lực học phân tử
MD được tiến hành trong thời gian là 20 ns (nano giây) bằng phần mềm GROMACS 2023.3 với trường lực CHARMM27 [18]. Đánh giá kết quả MD dựa trên các giá trị sau:
- Độ ổn định của protein tự do và phức hợp (RMSD) được tính trên mạch chính (backbone) của protein, cấu trúc được xem là ổn định và có ý nghĩa khi RMSD < 0,3 nm [19];
- Độ linh động của acid amin và phối tử trong hệ (RMSF). RMSF < 0.3 nm cho thấy nguyên tử hay phân tử ít dao động, ổn định [20];
- Khả năng duy trì cấu trúc không gian của protein (Rg) [21];
- Liên kết hydro được tạo thành trong quá trình mô phỏng [21].
III. Kết quả nghiên cứu:
3.1. Kết quả docking Acarbose trên enzym α-glucosidase
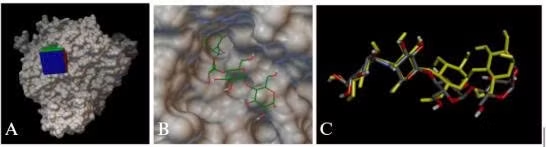
Enzym α-glucosidase (PDB ID: 2QMJ) chứa ligand đồng kết tinh là Acarbose gắn vào khoang tác động với năng lượng gắn kết là -7.4 kcal/mol (Hình 3.1 A, B). So sánh cấu trúc của ligand trước và sau khi gắn cho thấy không có sự khác biệt đáng kể, với giá trị RMSD là 1.90 Å (Hình 3.1 C). Đồng thời phân tích tương tác giữa ligand đồng kết tinh với protein cho thấy Acarbose có thể tạo được các liên kết hydro với các acid amin Asp203, Asp327, Asp443, Arg526, Asp542, His600 - những acid amin quan trọng quy định hoạt tính ức chế enzym giống như cấu trúc thực nghiệm [9].
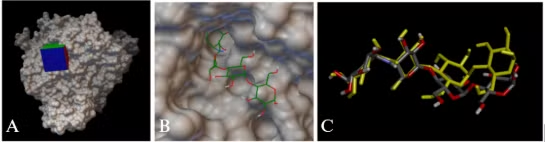
Hình 3.1. A.B. Cấu trúc không gian của enzym α-glucosidase với Acarbose ở vị trí hoạt động; C. Ligand Acarbose: trước khi redock (màu xám), sau khi redock (màu vàng)
Bảng 3.1 Kết quả re-docking các ligand đồng kết tinh vào cấu trúc protein
| Ligand | Tương tác trước re-docking | Tương tác sau re-docking |
| 2QMJ | Asp203, Thr207, Tyr299, Asp327, Trp406, Met444, Arg526, Asp542, Phe575, His600 | Asp203, Asn207, Tyr299, Asp327, Trp406, Asp443, Met444, Arg526, Asp542, Phe575, His600 |
3.2. Kết quả sàng lọc qua mô hình docking enzym α-glucosidase
Thực hiện docking 254 hợp chất từ cây Súng đỏ lên enzym α-glucosidase với chứng dương là Acarbose, kết quả cho thấy điểm docking dao động từ -10 đến -3.7 kcal/mol. Có 111 hợp chất đạt điểm gắn kết tương đương hoặc thấp hơn Acarbose (-7.4 kcal/mol).
3.3. Đánh giá ADMET
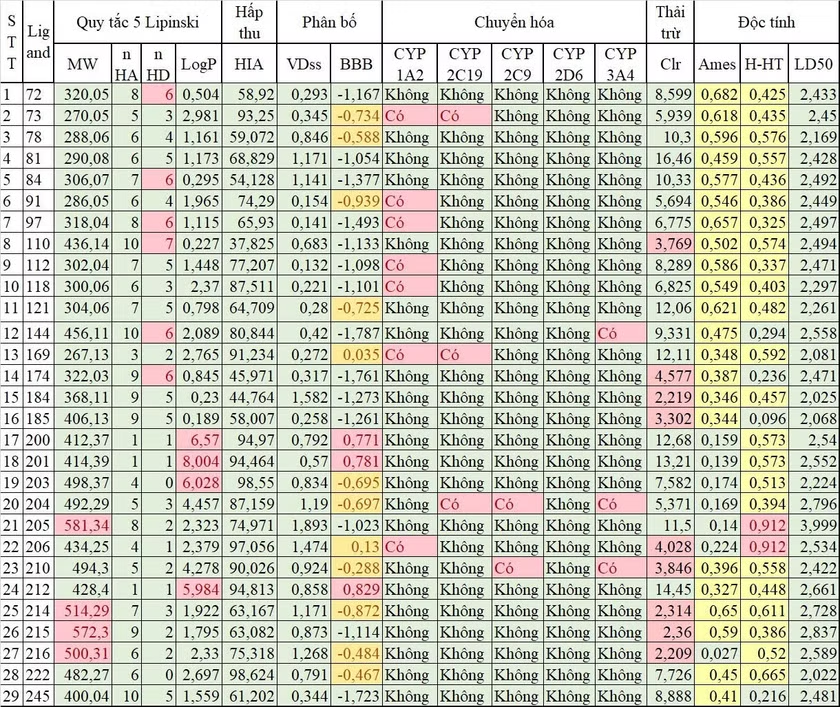
Các hợp chất có điểm số docking đạt yêu cầu tiếp tục được sàng lọc bằng cách đánh giá các đặc tính giống thuốc thông qua quy tắc 5 Lipinski, hấp thu, phân bố, chuyển hóa, thải trừ và các yếu tố độc tính. Qua sàng lọc còn lại 29 chất đáp ứng các tiêu chí và được chọn để mô phỏng động lực học phân tử (Phụ lục 1).
3.4. Mô phỏng động lực học phức hợp với enzym α-glucosidase
Để đánh giá tính ổn định và cấu hình của phức hợp protein-ligand, mô phỏng động lực học phân tử 20 ns được thực hiện bằng GROMACS 2023.3 (CHARMM27, 300K, 1 bar) trên 12 chất đã qua sàng lọc. Các thông số RMSD, RMSF, Rg và liên kết hydro được phân tích. Biểu đồ RMSD cho thấy các phức hợp ổn định nhất là ligand 81 (Catechin), 91 (Kaempferol), 97 (Myricetin) và 144 (Epicatechin methylgallate) với RMSD trung bình < 0.3 nm.
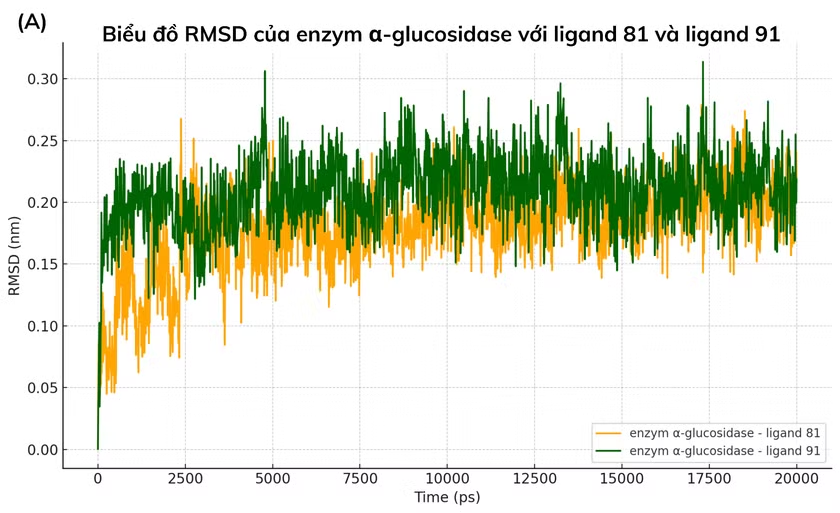
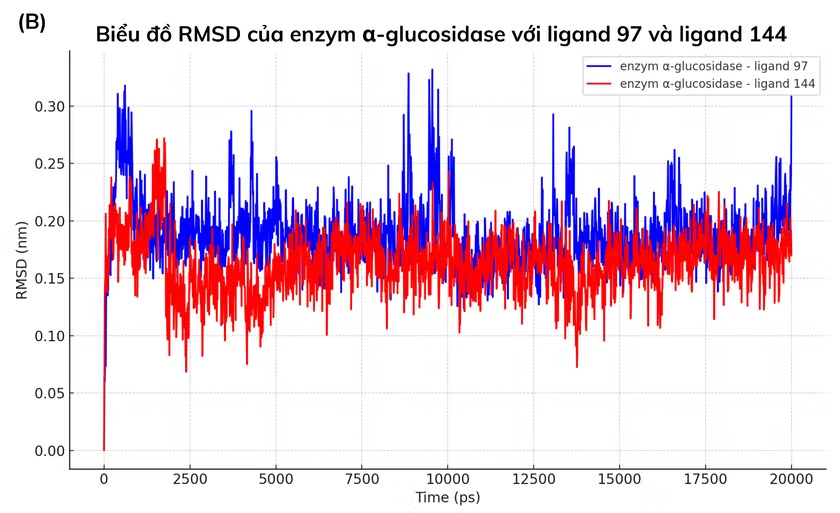
Phân tích RMSD trong suốt 20 ns mô phỏng cho thấy sự ổn định cấu trúc khác nhau giữa các phức hợp enzym α-glucosidase–ligand. Từ hình 3.2, ligand 144 biểu hiện độ ổn định cao nhất (0.1629 ± 0.0266 nm), tiếp theo là ligand 81 (0.1793 ± 0.0355 nm) và ligand 97 (0.1887 ± 0.0294 nm). Ligand 91 có RMSD trung bình cao nhất (0.2091 ± 0.0296 nm), phản ánh mức dao động lớn hơn và trạng thái ổn định kém hơn so với các ligand còn lại.
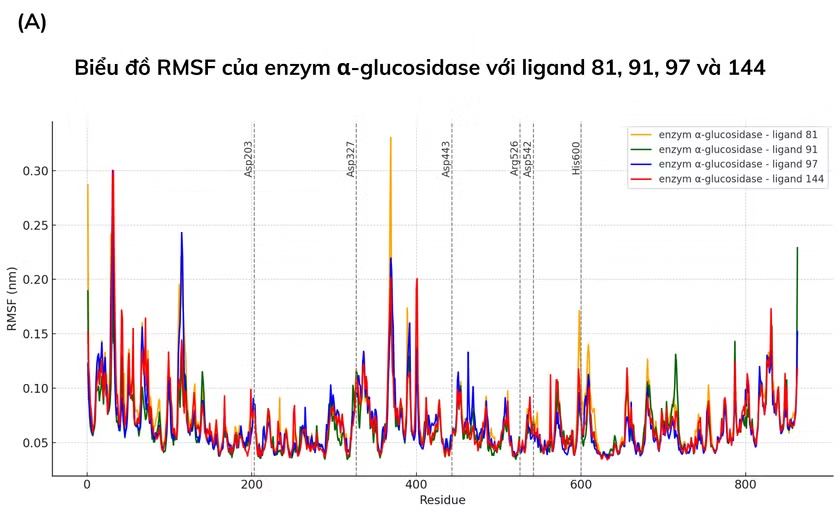
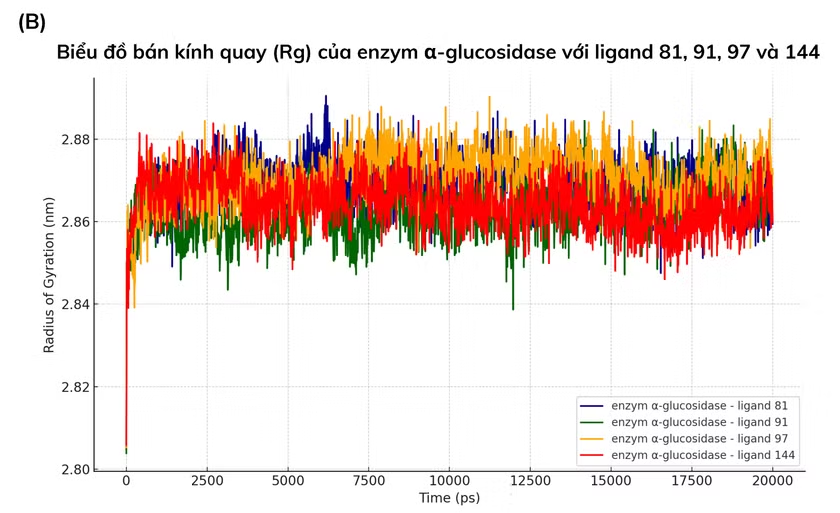
Giá trị RMSF cao nhất của các phức hợp α-glucosidase–ligand 81, 91, 97 và 144 lần lượt là 0.3304, 0.2291, 0.3002 và 0.2999 nm (Hình 3.3 A). 6 acid amin quan trọng (Asp443, Asp203, Asp327, Asp542, His600, Arg526) đều có RMSF thấp hơn đáng kể, cho thấy độ ổn định cao tại vùng hoạt động. Bán kính quay (Rg) của các phức hợp dao động ổn định trong khoảng 2.80–2.89 nm (Hình 3.3 B). Toàn bộ quá trình mô phỏng cho thấy các phức hợp duy trì cấu trúc ổn định trong suốt 20 ns.
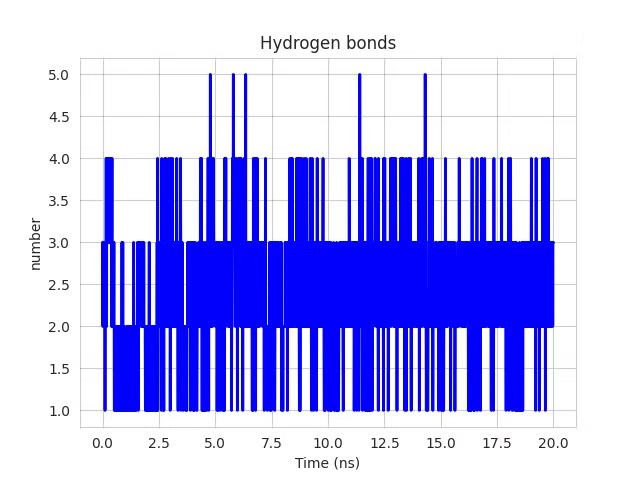 (A) | 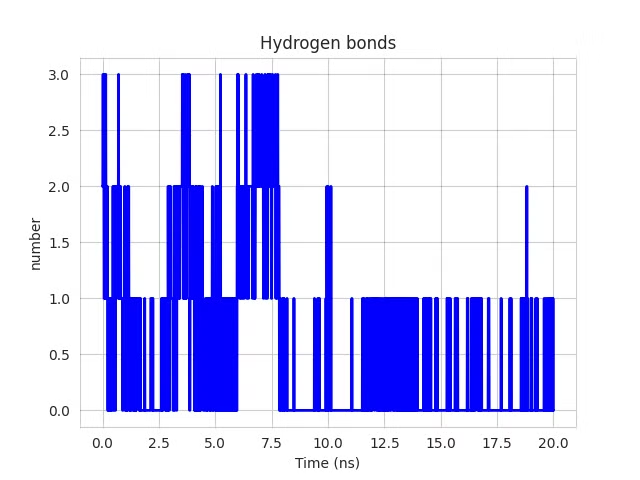 (B) | 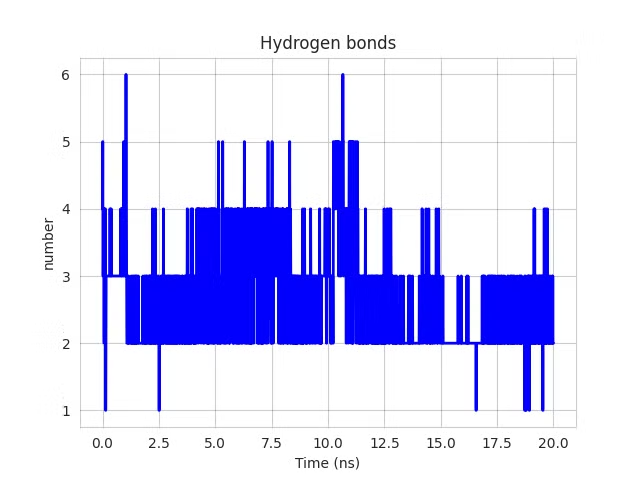 (C) | 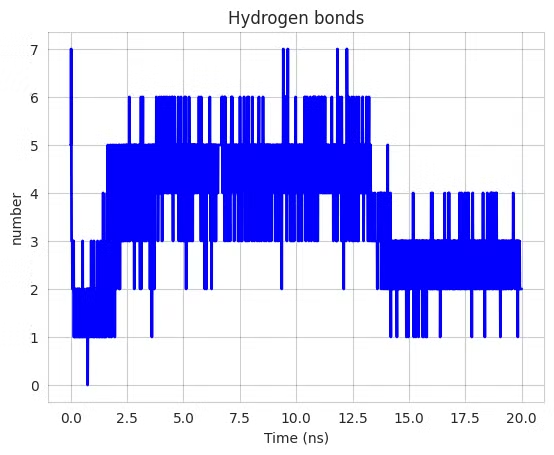 (D) |
| Hình 3.4. Số liên kết hydro theo thời gian của enzym α-glucosidase với ligand 81(A), 91(B), 97(C), 144(D). | |||
Số liên kết hydro là chỉ số quan trọng đánh giá mức độ tương tác giữa enzyme và ligand. Hệ enzym α-glucosidase–ligand 81 duy trì ổn định 44.73% thời gian (trung bình 2.40 liên kết), trong khi ligand 91 thể hiện tương tác yếu (trung bình 0.56 liên kết, 1.55% thời gian). Ligand 97 tương tác tốt hơn (trung bình 2.66 liên kết, 52.37% thời gian). Ligand 144 nổi bật với trung bình 3.63 liên kết và 76.81% thời gian ổn định, cho thấy ái lực và độ bền cao nhất (Hình 3.4).
IV. BÀN LUẬN
4.1 Catechin và Epicatechin methylgallate (ligand 81 và ligand 144)
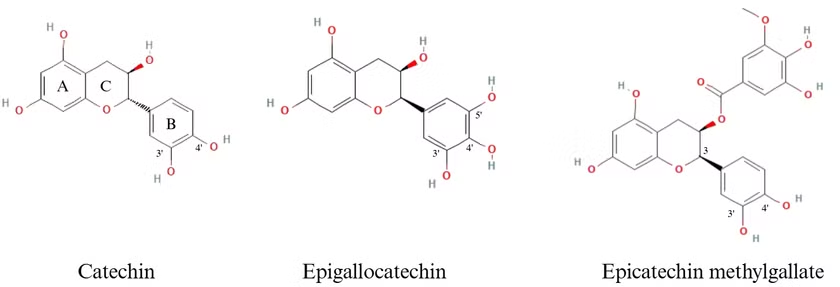
Hình 4.1. Cấu trúc của Catechin và các dẫn xuất
Catechin (ligand 81) có năng lượng gắn kết tương đương với Acarbose (-7.4 kcal/mol) và hình thành ba liên kết hydro với các acid amin quan trọng như Asp542, Asp203 và Asp327 thông qua nhóm hydroxy ở nhân chroman và cấu trúc 3’,4’-OH trên vòng B (Hình 4.1). Nhóm 4'-OH trên vòng B (Hình 4.1) được chứng minh là đóng vai trò quan trọng trong ức chế enzym α-glucosidase và hiệu quả tăng khi có thêm tương tác tại vị trí này. Ngoài ra, số lượng và vị trí của nhóm -OH trên vòng B (Hình 4.1) cũng ảnh hưởng đến hoạt tính [22]. Tuy nhiên, việc thêm nhóm -OH trên vòng B không phải lúc nào cũng tăng hiệu quả ức chế. Epigallocatechin - một chất trong cây Súng đỏ có thêm nhóm 5’-OH trên vòng B (Hình 4.2) so với cấu trúc của Catechin nhưng không tạo được tương tác nào tại vị trí này cũng như cho hoạt tính yếu. Theo một nghiên cứu của Lijun Sun cho thấy, ở nồng độ 1 mg/mL, tỷ lệ ức chế của Epigallocatechin chỉ dưới 20%, trong khi Catechin đạt gần 100% [23]. Ngoài liên kết hydro, Catechin còn hình thành liên kết pi-anion với Asp443 - cùng với Asp542 đã được nhiều nghiên cứu chỉ ra chúng là các mục tiêu quan trọng trong quá trình thủy phân liên kết 1,4-α-D-glucose của carbohydrat, trong đó Asp443 đóng vai trò xúc tác nucleophil và Asp542 vai trò xúc tác acid hoặc base [9], [24].
Epicatechin methylgallate (ligand 144) cho kết quả docking vượt trội hơn Acarbose với giá trị đạt -8.2 kcal/mol, đây là phối tử có điểm số tốt nhất sau khi lọc qua các chỉ số ADMET và Lipinski. Bên cạnh đó, số lượng liên kết hydro duy trì trong quá trình mô phỏng động lực học phân tử kéo dài 20 ns là một trong những chỉ số quan trọng phản ánh tính ổn định thực của tương tác và kết quả vượt trội của Epicatechin methylgallate cũng thể hiện ở chỉ số này. Catechin có số liên kết hydro trung bình 2.4, với giá trị cao nhất đạt 5, trong khi đó Epicatechin methylgallate có số liên kết hydro trung bình 3.63, với giá trị cao nhất lên đến 7. Kết quả này cho thấy Epicatechin methylgallate có ái lực và liên kết ổn định nhất trong các phối tử. Điều này có thể được lý giải bởi Epicatechin methylgallate có nhóm galloyl tại vị trí 3-OH góp phần tăng khả năng ức chế enzym α-glucosidase, được nhắc đến trong nghiên cứu của Lijun Sun [9].
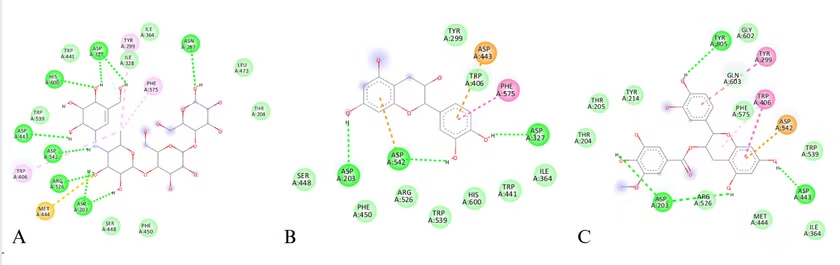
Hình 4.2. Tương tác với acid amin trên α-glucosidase của Acarbose(A), ligand 81(B) và ligand 144 (C). Trong đó: liên kết hydro (màu xanh đậm), liên kết pi-anion (màu cam), liên kết pi-pi (màu hồng đậm), liên kết pi-alkyl (màu hồng nhạt) liên kết Van der Waals (màu xanh nhạt).
Hai hợp chất Catechin và Epicatechin methylgallate đều thể hiện đặc tính dược động học thuận lợi. Cả hai có khả năng hấp thu qua đường ruột tốt, đặc biệt Epicatechin methylgallate đạt HIA 80,844%, cao hơn Catechin (68,829%). Về chuyển hóa, Catechin không ức chế bất kỳ enzyme CYP nào trong số 5 CYP chính, trong khi Epicatechin methylgallate ức chế CYP3A4, tiềm ẩn nguy cơ tương tác thuốc. Catechin có tốc độ thải trừ nhanh nhất trong các chất được xét (16,455 ml/phút/kg), điều này có thể ảnh hưởng đến thời gian tác dụng và cần cân nhắc khi thiết kế liều. Cả hai đều không gây đột biến gen và có độc tính cấp thấp với LD₅₀ > 2 mol/kg; Epicatechin methylgallate an toàn hơn với gan (H-HT=0,294). Nhìn chung, hai hợp chất cho thấy tiềm năng ứng dụng trong điều trị đái tháo đường type 2, tuy nhiên cần thêm các nghiên cứu in vitro và in vivo để xác nhận hiệu quả cũng như độ an toàn trên sinh vật sống.
4.2.2. Kaempferol và Myricetin (ligand 91 và ligand 97)
Trong nghiên cứu của Hui C [25] và Normah H [26], cả Myricetin và Kaempferol đều thể hiện khả năng ức chế α-glucosidase, nhưng Myricetin vượt trội hơn với tỷ lệ ức chế 94% (so với 82% của Kaempferol). Phân tích in silico Myricetin có năng lượng liên kết thấp hơn Kaempferol (-7.6 kcal/mol so với -7.4 kcal/mol) và với đề tài nhóm nghiên cứu cũng cho kết quả tương tự. Phức hợp giữa α-glucosidase và Myricetin có năng lượng liên kết -8.0 kcal/mol và Kaempferol là -7.4 kcal/mol, trong khi đó chứng dương Acarbose đạt -7.4 kcal/mol. Hai acid amin quan trọng trong hoạt động thủy phân của enzym α-glucosidase (Asp443 và Asp542) được cả Myricetin và Kaempferol tương tác nhưng lại khác loại liên kết lần lượt là liên kết hydro và Van der Waals. Còn với Asp542, cả 2 ligand đều hình thành liên kết π-anion tại nhân chromone.
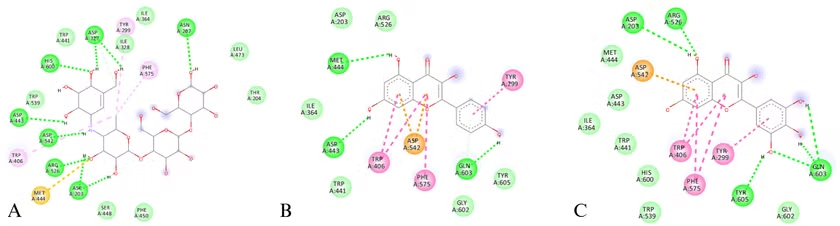
Hình 4.3. Tương tác với acid amin trên α-glucosidase của Acarbose(A),ligand 91(B),ligand 97(C)
Một nghiên cứu cho thấy sự phối hợp giữa nhóm C4=O và hệ liên hợp C2=C3 trong vòng C đóng vai trò then chốt trong cơ chế ức chế, từ đó tăng cường khả năng ức chế α-glucosidase của Myricetin [25]. Thêm vào đó, Myricetin có các nhóm hydroxy liền kề trên vòng B (3′,4′,5′-OH), tại đó các liên kết hydro được hình thành. Đối với Kaempferol chỉ có 1 nhóm 4′-OH tại vòng B và các liên kết hydro được hình thành giữa nhóm hydroxy đơn lẻ trên vòng A hoặc C của nó. Đây có thể là lý do cho thấy Myricetin và Kaempferol có cấu trúc khá giống nhau nhưng tác dụng ức chế α-glucosidase có sự chênh lệch.
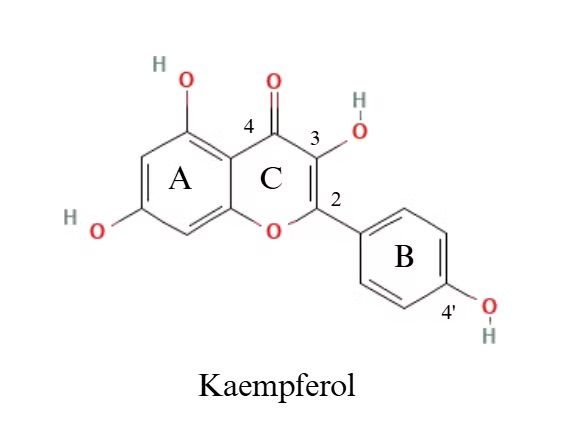
Hình 4.4. Cấu trúc của Kaempferol và Myricetin
Xét đến chỉ số liên kết hydro trong quá trình mô phỏng động lực học phân tử, Kaempferol có số liên kết hydro trung bình chỉ 0.56, với giá trị cao nhất đạt 3, trong khi đó, Myricetin có kết quả hơn rõ rệt với số liên kết trung bình đạt 2.66 và số liên kết tối đa lên đến 6. Điều này cho thấy Myricetin không chỉ có ái lực mạnh hơn mà còn duy trì trạng thái gắn kết bền vững hơn so với Kaempferol.
Về ADMET cả hai ligand đều có các thông số tương đối tốt: khả năng hấp thu ở ruột lớn hơn 60%, không qua hàng rào máu não, an toàn với giá trị LD50>2 mol/kg, không gây đột biến gen. Tuy nhiên, do ức chế CYP1A2 và có khả năng gây độc tính gan, cần lưu ý nguy cơ tương tác thuốc và tiến hành thêm các nghiên cứu để làm rõ mối liên hệ giữa độc tính với tác dụng ức chế enzym α-glucosidase, cũng như tiềm năng phát triển thành thuốc của hai hợp chất.
V. Kết luận
Qua quá trình nghiên cứu, đề tài đã đạt được các kết quả sau:
- Hoàn thành docking 254 hợp chất được phân lập từ cây Súng đỏ lên enzym α-glucosidase, thu được 111 chất có điểm số docking tương đương và tốt hơn Acarbose.
- Thông qua đánh giá ADMET có 29 chất được chấp thuận theo quy tắc Lipinski, đánh giá hấp thu, phân bố, chuyển hóa, thải trừ và độc tính.
- Mô phỏng động lực học phân tử 20ns thu được 4 chất tiềm năng là Catechin (ligand 81), Kaempferol (ligand 91), Myricetin (ligand 97) và Epicatechin methylgallate (ligand 144).
VI. Kiến nghị
Các định hướng đề tài được tiếp tục:
- Tối ưu hóa cấu trúc tiềm năng, để tăng hiệu lực và cải thiện đặc tính ADMET.
- Thực hiện nghiên cứu in vitro trên tế bào để kiểm tra hiệu quả ức chế của các hợp chất đối với enzym α-glucosidase.
- Thực hiện các thử nghiệm in vivo trên mô hình động vật để đánh giá tính an toàn và hiệu quả điều trị của ứng viên tiềm năng.
VII. Tài liệu tham khảo
- Ngoc NB, Lin ZL, Ahmed W, et al. Diabetes: What challenges lie ahead for Vietnam? Ann Glob Health. 2020;86(1):1–9.
- Bộ Y tế. Quyết định về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị đái tháo đường típ 2”. 2020;5481/QĐ-BYT.
- Yang CY, Yen YY, Hung KC. Inhibitory effects of pu-erh tea on alpha glucosidase and alpha amylase: a systemic review. Nutr Diabetes. 2019;9(23):1–6.
- Rocha S, Sousa A, Ribeiro D, Correia CM, et al. A study towards drug discovery for the management of type 2 diabetes mellitus through inhibition of the carbohydrate hydrolyzing enzymes α-amylase and α-glucosidase by chalcone derivatives. Food Funct. 2019;9(10):5510–5520.
- Naznin M, Alam MB, Alam R, et al. Metabolite profiling of Nymphaea rubra (Burm. f.) flower extracts using cyclic ion mobility–mass spectrometry and their associated biological activities. Food Chem. 2023;404:134544.
- Ishrat N, Gupta A, Khan MF, et al. Phytoconstituents of Nymphaea rubra flowers and their anti-diabetic metabolic targets. Fitoterapia. 2024;176:106014.
- Naznin M, Alam MB, Lee SH, et al. Optimizing ultrasonic-assisted extraction and untargeted metabolite identification from red water lily (Nymphaea rubra) leaves with enhanced antioxidant activity. Food Chem Adv. 2024;100696:1–11.
- Protein Data Bank [Internet]. Available from: https://www.rcsb.org/docs/general-help/ organization-of-3dstructures-in-the-protein-data-bank [cited 2024 Sep 18].
- Sim L, Quezada-Calvillo R, Sterchi EE, et al. Human intestinal maltase glucoamylase: crystal structure of the N-terminal catalytic subunit and basis of inhibition and substrate specificity. J Mol Biol. 2008;375(3):782–792.
- PubChem [Internet].Available from:https://pubchem.ncbi.nlm.nih.gov/[cited 2024 Sep 14].
- Trott O, Olson AJ. AutoDock Vina: improving the speed and accuracy of docking with a new scoring function, efficient optimization, and multithreading. J Comput Chem. 2010;31(2):455–461.
- Meng XY, Zhang HX, Mezei M, Cui M. Molecular docking: a powerful approach for structure-based drug discovery. Curr Comput Aided Drug Des. 2011;7(2):146–157.
- Setiawansyah A, Reynaldi MA, Tjahjono DH. Molecular docking-based virtual screening of antidiabetic agents from Songga (Strychnos lucida R.Br.): an Indonesian native plant. Curr Res Biosci Biotechnol. 2022;3(2):208–214.
- Yohana V, Wijianto B, Arief I. Molecular docking study of epigallocatechin gallate (EGCG) as a therapy for type 2 diabetes mellitus. J Kimia Riset. 2024;1(9):46–58.
- Zamudio FV, Hidalgo-Figueroa SN, Ortíz RR. Identification of antidiabetic peptides derived from in silico hydrolysis of three ancient grains: Amaranth, Quinoa and Chia. Food Chem. 2022;394:133479.
- ADMETlab [Internet]. Available from: https://admetmesh.scbdd.com/ [cited 2024 Sep 14].
- pkCSM [Internet]. Available from: https://biosig.lab.uq.edu.au/pkcsm/prediction [cited 2024 Sep 14].
- GROMACS Tutorials [Internet]. Available from: http://www.mdtutorials.com/gmx/ [cited 2024 Sep 14].
- Reva BA, Finkelstein AV, Skolnick J. What is the probability of a chance prediction of a protein structure with an rmsd of 6 Å? Fold Des. 1998;3(2):141–147.
- Jülich F. Analysis of MD Simulations [Internet]. Available from: http://www.drugdesign.gr/uploads/7/6/0/2/7602318/lecture_mdanalysis.pdf [cited 2024 Sep 14].
- Abraham M, Hess B, van der Spoel D, et al. GROMACS Reference Manual [Internet]. 2017. Available from: https://manual.gromacs.org/5.1-current/manual-5.1.5.pdf [cited 2024 Sep 14].
- Zhang LL, Liu J, Wang X, et al. The mechanism of interactions between flavan-3-ols against α-glucosidase and their in vivo antihyperglycemic effects. Bioorg Chem. 2019;85:364–372.
- Sun L, Zhang H, Guo Y, et al. The galloyl moiety enhances the inhibitory activity of catechins and theaflavins against α-glucosidase by increasing the polyphenol–enzyme binding interactions. Food Funct. 2021;12(1):215–229.
- Elhady SS, Alshobaki NM, Elfaky MA, et al. Deciphering Molecular Aspects of Potential α-Glucosidase Inhibitors within Aspergillus terreus: A Computational Odyssey of Molecular Docking-Coupled Dynamics Simulations and Pharmacokinetic Profiling. Metabolites. 2023;13(8):942.
- Hui C, Xiaoqing C. Structures required of flavonoids for inhibiting digestive enzymes. Anticancer Agents Med Chem. 2012;12:929–939.
- Normah H, Norsyarina N, Nor Aini A, et al. Molecular docking of polyphenol compounds from Anacardium occidentale with alpha-glucosidase and dipeptidyl peptidase-4 enzymes. Malays J Fundam Appl Sci. 2021;17:202–216.
PHỤ LỤC 1